Sådan undgår du korrosion
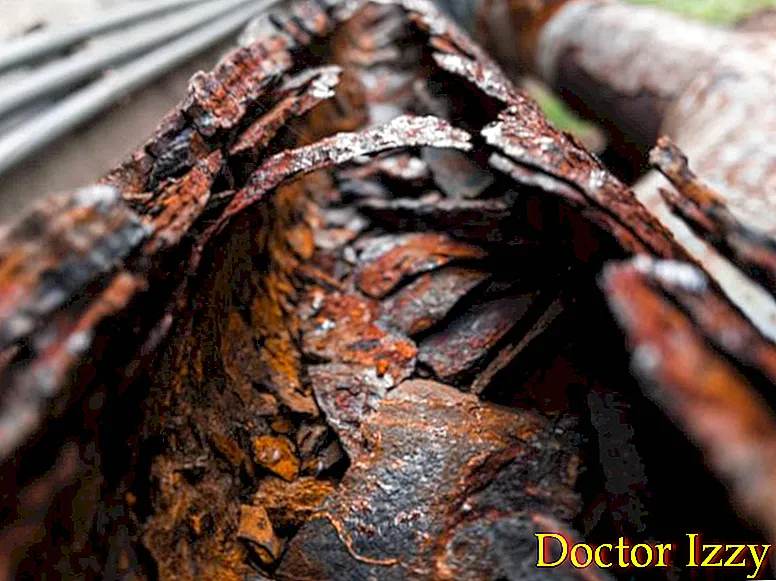
Ved kontakt med ilt begynder metaller at korrodere. Dette sker, når iltatomer bryder bindingen af atomer i metaller. Korrosionsprocessen begynder, når metallet kommer i kontakt med det omgivende miljø og begynder at miste sin struktur og egenskaber, både fysiske og kemiske.
Kan korrosion forhindres, så metaller holder meget længere? Har du haft eller opdaget korrosionsproblemer i dit hjem, køretøj eller arbejdsplads? I oneHOWTO forklarer vi hvordan man undgår korrosion og oxidation i metaller såsom galvanisk, jern og stål. Gå efter det!
Indeks
- Hvad er korrosion og oxidation
- Sådan undgår du galvanisk korrosion
- Sådan undgår du korrosion i jern
- Sådan undgår du korrosion af stål
Hvad er korrosion og oxidation
Korrosion og oxidation er to processer, der skader metaller, selvom de er lidt forskellige, og reducerer levetiden for mange af de objekter, vi bruger dagligt. I dette afsnit forklarer vi, hvad korrosion og oxidation er, deres årsager og virkninger samt de typer miljøer, der genererer denne proces.
Hvad er korrosion
Fænomenet korrosion henviser til forringelsen af et metal på grund af et eksternt kemisk eller elektrokemisk angreb. På denne måde frigiver materialet elektroner, når det er i nærværelse af en elektrolyt eller reaktant, såsom vand eller ilt. I tekniske termer går metaller fra en anodisk region til en katodisk region. Metalkorrosion forekommer i det anodiske område, og dets forurening og reduktion sker i det katodiske område.
Korrosion er ikke et fænomen, der udelukkende findes i metaller, da det også påvirker andre materialer såsom keramik og glas. Det er også til stede i plast, hvis fænomen er kendt som polymernedbrydning. Derudover påvirker disse processer miljøet, både atmosfæren og vandet.
Hvad er oxidation
Oxidation repræsenterer derimod det fænomen, der producerer korrosion af metaller, når reaktanten udelukkende er ilt, som generelt kommer fra vand eller luft. Oxidation er den kemiske reaktion, der skyldes kombinationen af ilt med andre materialer og stoffer, hvilket resulterer i oxidmolekyler, der korroderer materialer. Korrosion opstår på grund af tab af elektroner i atomer af materialer, der er positivt ladede.
Oxygen kaldes et oxidationsmiddel, fordi det vinder elektroner, mens materiale, der mister elektroner, kaldes et reduktionsmiddel. I denne proces reduceres ilt, fordi det vinder elektroner, og materialet oxiderer, fordi det mister elektroner.
Undertiden sker oxidation med vilje i industrier. For eksempel ekstraheres aluminium, som findes i naturen som bauxit, fra en elektrolyseproces, hvor aluminiumoxid adskilles fra aluminium i sin rene tilstand.
Typer af ætsende miljøer
Der er forskellige typer miljøer, der producerer korrosion. Blandt dem, vi kan nævne, er:
- Atmosfærisk: dets vigtigste oxidationsmidler er ilt og vand. Det dækker de fleste af de ætsende miljøer, da det er til stede over hele planeten.
- Marine: det er kendetegnet ved tilstedeværelsen af saltvand, som det sker i havene eller havene. Saltvand indeholder klor, et stærkt ætsende middel.
- Industriel: dette miljø er meget ætsende på grund af dets store mængde forurenende og ætsende gasser og væsker. Nogle af dem er blandt andet svovlholdige og nitrøse materialer.
- Galvanisk: opstår, når et metal kommer i kontakt med et andet mere ædelt metal (metaller, der genererer ringe kemisk reaktion og ikke er meget modtagelige for korrosion), og begge nedsænkes i en elektrolyt eller et vådt medium.
Nogle genstande såsom batterier er ofte meget modtagelige for korrosion og oxidation. Besøg vores artikel Sådan rengøres korroderede battericeller for at lære mere.
Sådan undgår du galvanisk korrosion
Det galvanisk korrosion Det forekommer mellem to metaller af forskellig art, der kommer i kontakt, mens de nedsænkes i en elektrolyt såsom saltvand. Dette resulterer i en elektrokemisk proces, der producerer korrosion.
EN eksempel på galvanisk korrosion det forekommer især i havmiljøer eller ved kysterne. Placering af metaller, der ikke er meget modtagelige for korrosion ved siden af meget modtagelige metaller, fremskynder korrosionsprocessen for det modtagelige metal. Det forekommer normalt i bølgepap, når zinket, der beskytter det, går i stykker.Det er også sket i nogle skibe, da jernspik blev brugt til at fastgøre kobberet på dækket til træet. Kobber korroderer hurtigere, hvis de kommer i kontakt med jern i havvand.
Til undgå galvanisk korrosion, kan du følge metoderne og teknikkerne, som vi beskriver nedenfor:
- Isoler kontaktpunkterne mellem metallerne ved hjælp af plast- eller gummiisolerende materiale.
- Anbring offerelektroder som zink og magnesium, så det er dem, der korroderer og kan udskiftes, når de bæres. Denne proces er kendt som katodisk beskyttelse.
- Undgå at bruge materialer, der har forskellige niveauer af elektrokemisk potentiale.
- Dæk kontaktområder med isolerende maling.
- Brug galvaniseringsteknikken: belæg metallet med en elektrolyt som sølv eller nikkel.
Ser du rust på din cykel, motorcykel eller køretøj? I oneHOWTO fortæller vi dig, hvordan du fjerner rust fra motorcyklen, så den ser ud som ny.
Sådan undgår du korrosion i jern
Jern repræsenterer det fjerde element o mest rigelige materiale på jorden. Dets symbol i det periodiske system er Fe, og det er et ferromagnetisk materiale. Det ekstraheres direkte fra minerne og behandles i stålværkerne. Som alt metal udsættes det for fænomenet oxidation.
Nogle af de genstande, vi bruger dagligt og er lavet af jern, er værktøjer såsom hamre, skruer og møtrikker samt nøgler, døre, gelænder, vinduesrammer, stolestel, mekaniske arme og gear. Til forhindre korrosion på jern, kan du bruge følgende metoder:
- Coat jernet med antioxidantsprays, der reagerer på ætsende stoffer.
- Beskytter jern med aktive metaller. Brug legeringer, der ændrer det kemisk, ligesom rustfrit stål kan.
- Coat strygejernet med et vandtæt lag maling for at forhindre det i at komme i kontakt med luft og vand.

Sådan undgår du korrosion af stål
Stål er et metal, der er fremstillet af kombinationen af jern og kulstof. Imidlertid har stål også en tendens til at ruste. Denne proces begynder, når stålet udsættes for ilt, som dannes jernoxid. Når dette fænomen opstår, får stålet en rødlig farve. Over tid vil dette forringe overfladen af stålet, efterlade det udsat og starte korrosionsprocessen.
Nogle af de hverdagslige genstande, der er lavet af stål, inkluderer skruer, søm, madredskaber eller bildele. Til forhindre korrosion af stål, kan du bruge følgende antioxidantteknikker eller processer, der er ideelle til stål:
- Udfør katodisk beskyttelse med zinkanoder eller belæg den med zink.
- Belæg stålet med plast.
- Coat eller mal stålet med rustbeskyttende maling.
- Du kan også bruge rustfrit stål, lavet af krom, silicium og mangan.
- Gennemgå en grundingsproces. Dette består i at belægge stålet med en slags korrosionsbeskyttende maling. Hvis stålet skal bruges udendørs, skal du bruge calciumfiber, og hvis du skal bruge det indendørs, skal du belægge med zinkchromat.
Hvis du har problemer med rust i din vask, skal du finde ud af, hvordan du kan rengøre og vedligeholde den i vores artikel Sådan fjernes rust fra en køkkenvask.

Hvis du vil læse flere artikler, der ligner Sådan undgår du korrosion, vi anbefaler, at du indtaster vores kategori af hjemmevedligeholdelse og sikkerhed.